今天给大家分享一篇Chemical science上的文章,本文的通讯作者来自卡迪夫大学化学学院Louis Y. P. Luk教授,该课题组的研究兴趣为旨在使用先进的化学生物学和合成生物学技术来解决医学上重要的酶学问题。

蛋白质生物连接中已经有了巨大的扩展,包括了生物化学和有机化学的传统方法的联合运用。天冬酰胺基内肽酶(AEP)是肽和蛋白质标记的酶学方法。OaAEP1是一种重要的AEP酶,其最大的特点在于其出色动力学特性和相对较短的识别序列(3个氨基酸,P1-P1’-P2’)。同时,AEP有相对宽松的底物特异性,其已被用于改善酶催化的生物连接反应。目前已经报道了各种方法来促进反应的进行,包括使用硫代二肽和自组装蛋白结构域的方法来提高反应性。但是,这些都需要大量的标记剂来实现反应的进行,这成为昂贵或非商业可用标记(例如同位素,放射性和荧光标记)的主要障碍。之前有研究表明, OaAEP1可以识别Asn-Cys-Leu(P1-P1’-P2’)进行连接,但是这样的反应将生成带有N端半胱氨酸(Cys-Leu)的副产物,这样的产物具有一定的反应活性。2-甲酰基苯基硼酸(FPBA)是一种亲电子试剂,可与N端半胱氨酸反应,具有出色的选择性和效率,可以用作具有N端半胱氨酸的肽段和连接。考虑FPBA和N端半胱氨酸之间形成的非天然仲胺基序不太可能是AEP催化的反应底物,因此,通过添加FPBA也许可以捕获酶促反应Cys-Leu的副产物,从而实现不可逆的AEP标记系统。在这里,作者开发了化学酶蛋白标记策略,通过AEP的分子间连接与FPBA反应偶联,实现位点特异性标记各种蛋白质的N-或C-末端。其中,AEP标记的P1-P1’-P2’识别序列为Asn-Cys-Leu,而FPBA作为清除剂,它与生成的产物Cys-Leu的1,2-氨基硫醇基序反应,可以进一步推动AEP介导的肽连接,同时减少使用的标记试剂的量。

然而,AEP存在着一个副反应:AEP能够使用水作为亲核试剂来催化天冬酰胺(和天冬氨酸)残基的水解,这会造成标签序列,底物或产物被水解,从而产生不必要的副产物。因此作者使用肽LFRANCLK和GLGGIR之间的分子间连接反应作为模型,进行几个关键变量的筛选,以降低OaAEP1的水解反应影响。作者测试的100个多肽反应,筛选了pH值、反应时间和亲核肽等反应条件,在确保最低的副反应的效率下,得到了最佳的反应条件:当系统中包含FPBA时,使用1.2当量亲核肽,在pH 5.7的4小时内,可得到94%的连接产物LFRANGLGGIR。相反,当排除FPBA时,产物转化率停在50%。对于无半胱氨酸的肽LFRANALK,添加FPBA时未观察到连接产率的显着差异。总之,这些观察结果表明反应产率的增加是由FPBA反应和AEP连接之间的偶联引起的。

作者将新开发的方法用于特定位置的C末端标记,将包含Asn-Cys-Leu的识别肽添加到eGFP的C末端,并与生物素化肽GLGGZ(其中Z为生物素化赖氨酸)进行连接反应。通过LC-MS分析当包含FPBA时,C端修饰的蛋白质的产率高达86%。同时,作者也在eGFP, beta-lactamase 、AaLS13和ubiquitin蛋白的C端或者N端修饰的蛋白质实现标记。
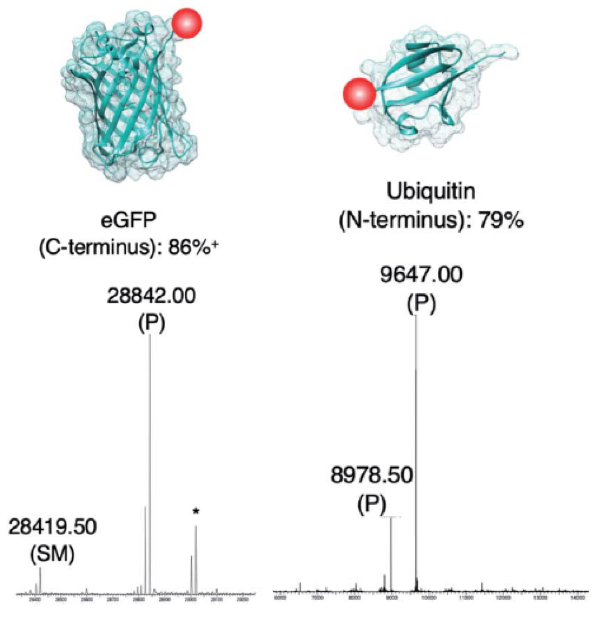
总之,AEP连接/ FPBA偶联系统可以实现位点特异性标记各种蛋白质的N-或C-端,该方法为制备定制的蛋白质构建体提供了一种通用而有效的方法。
本文作者:LSC
文章链接:https://pubs.rsc.org/en/content/articlepdf/2020/sc/d0sc02023k
文章引用:DOI: 10.1039/d0sc02023k








目前评论: